Nicht erst mit dem neuen Trend zur Digitalisierung auch im Bereich Medizintechnik kommen Verfahren um Hard- und Software für Medizintechnik und die Frage der CE-Zertifizierung für Medizinprodukte vor Gericht. EuGH und BGH urteilten bereits 2013 grundsätzlich dazu.
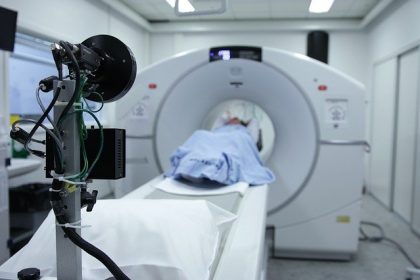 Einordnung als Medizinprodukt
Einordnung als Medizinprodukt
Ob ein Produkt eine Einordnung als Medizinprodukt erfordert, ist immer wieder sowohl strategische Entscheidung in der Medizintechnik als auch Streitpunkt vor Gericht. In einem für die Branche Medizintechnik maßgeblichen Fall ging es schon bereits 2013 um die den Einsatz von Hard- und Software für Medizintechnik und die Frage der CE-Zertifizierung für Medizinprodukte.
Konkret ging es um den Vertrieb des Systems „ActiveTwo“, mit dem bioelektrische Daten gemessen und aufgezeichnet wurden. Die Inhaberin dieses Systems, eine Gesellschaft niederländischen Rechts, betrieb für das System Werbung in Deutschland. Dagegen klagte ein Hersteller von Hard- und Software für Medizintechnik. Der Kläger machte geltend, es handele sich um irreführende Werbung, weil für das System der Beklagten weder in den Niederlanden noch in Deutschland eine CE-Zertifizierung für Medizinprodukte bestehe. Der Kläger führte an, dass alle Merkmale des § 3 Nr. 1 Buchst. c MPG für ein Medizinprodukt erfüllt seien, daher eine CE-Zertifizierung zwingend war.
Die Beklagte wies den Vorwurf zurück und verwies darauf, dass die zuständige niederländische Gesundheitsbehörde der Ansicht war, dass die Beklagte ihr System nicht zertifizieren zu lassen brauche, ergo der Vertrieb in Deutschland nicht durch das deutsche Wettbewerbsrecht eingeschränkt werde.
Das System „ActiveTwo“ weise nach der maßgeblichen Bestimmung der Beklagten als der Herstellerin keine für seine Einordnung als Medizinprodukt erforderliche Zweckbestimmung auf. Und auch die Tatsache, dass dieses System zu einem Diagnosegerät umgebaut werden könne, führe nicht zu seiner Einordnung als Medizinprodukt.
EuGH Entscheidung „Brain Products“
Letztlich führte diese gerichtliche Auseinandersetzung zu einer Vorlagefrage an das höchste Europäische Gericht (EuGH), das im November 2012 in seiner Entscheidung „Brain Products“ (C-219/11) ein wichtiges Urteil für Medizinprodukte traf: ein Gegenstand, der von seinem Hersteller zur Anwendung für Menschen zum Zwecke der Untersuchung eines physiologischen Vorgangs konzipiert wurde, könne demnach nur dann unter den Begriff „Medizinprodukt“ fallen, wenn der Gegenstand für einen medizinischen Zweck bestimmt ist (Auslegung von Art. 1 Abs. 2 Buchst. a 3. Gedankenstrich der Richtlinie 93/42/EWG, seit 2007 die Richtlinie 2007/47/EG).
BGH 2013: kein Medizinprodukt, wenn medizinischer Zweck ausgeschlossen
Der BGH nahm diese EuGH Entscheidung in sein abschließendes Urteil „Messgerät II“ auf und entschied den Fall gegen den Kläger. Wenn die Verwendung für einen medizinischen Zweck unmissverständlich ausgeschlossen wird, handelt es sich grundsätzlich um kein Medizinprodukt im Sinne von § 3 Nr. 1 MPG (Medizinproduktegesetz (MPG)), urteilte der BGH.
Das Gericht erläuterte, solange die Zweckbestimmung nach dem Verständnis des angesprochenen Verkehrs eindeutig ist und nicht willkürlich erscheint, insbesondere also eine nichtmedizinische Verwendung des Produkts ohne weiteres denkbar ist, könne der Hersteller demnach den Anwendungsbereich eines Produkts, das an sich sowohl medizinischen als auch nicht-medizinischen Zwecken dienen könnte, auf den nicht-medizinischen Bereich beschränken.
Mit Recht habe die Revisionserwiderung auf die Feststellung des Berufungsgerichts hingewiesen, der zufolge das System „ActiveTwo“ als solches für diagnostische oder therapeutische Zwecke objektiv nicht geeignet ist, ergänzte der BGH. Für einen diagnostischen Einsatz wäre es zumindest erforderlich, schloss das Gericht, dass ein Erwerber mit einem entsprechenden technischen Verständnis ein Konvertierungsprogramm installiert und zusätzlich Diagnoseprogramme Dritter einsetzt.
Fazit
Im Bereich Medizintechnik und Medizinprodukt ist der Unterschied zwischen dem Medizinproduktegesetz und dem Markengesetz dringlich zu beachten- denn für ein Medizinprodukt im Markenrecht gilt (anders als im Medizinproduktegesetz und im Übrigen auch anders als im Patentrecht): medizinischer Zweck ist nicht entscheidend.
Zu beachten ist auch, dass seit 2017 der Begriff „Medizinprodukt“ in den EU Verordnungen als Überbegriff sowohl für Produkte nach der Verordnung (EU) 2017/745 (MDR) als auch in der Verordnung (EU) 2017/746 (IVDR) verwendet wird. Insbesondere stellt Anhang XVI der MDR ein Verzeichnis von Produktgruppen dar, die sogar ohne medizinischen Zweck unter das Medizinprodukterecht gestellt sind, vor allem aus dem übergeordneten Bereich „Ästhetik“. Bei ihrer Verwendung darf – entsprechend ihrer Zweckbestimmung – kein Risiko oder kein höheres als das höchstzulässige Risiko bei der Anwendung ausgehen. Zudem gilt auch für die in Anhang XVI genannten Produkte ohne medizinische Zweckbestimmung ebenso wie für „klassische“ Medizinprodukte die Anforderung, einen klinischen Nutzen nachzuweisen.
Suchen Sie Beratung in Markenrecht, Patentschutz oder erweiterte Schutzzertifikate?
Unsere Patent- und Rechtsanwaltskanzlei verfügt über jahrelange Expertise im Schutz von Patenten, insbesondere auch im Bereich Pharma und Medizinprodukte, national wie auch international.
Bei Interesse nehmen Sie gerne Kontakt mit uns auf.

Quellen:
BGH Urteil „Messgerät II“, I ZR 53/09
Bild:






Schreiben Sie einen Kommentar